CBT-001目前正處於3期臨床試驗階段,以評估其治療翼狀胬肉的療效。這將是第一個治療翼狀胬肉的疾病改善、同類首創的藥物療法。
CBT-001 是一種能有效的抑制血管內皮生長因數受體 (VEGFRs)、血小板衍生生長因數受體 (PDGFRs)、成纖維細胞生長因數受體(FGFRs) 多激酶抑制劑,可抑制血管生成和纖維化。 CBT-001 是一種獨特的局部用藥制劑,正在通過 505b(2) 監管途徑開發,用於治療目前尚無獲批藥物治療的翼狀胬肉。目前 手術切除是翼狀胬肉患者的唯一選擇和護理標準治療。 通過藥理學針對已確立的翼狀胬肉的血管生成和纖維化發病機制的藥物療法,我們將阻止翼狀胬肉的生長惡化並減少無需進行切除手術的需要。
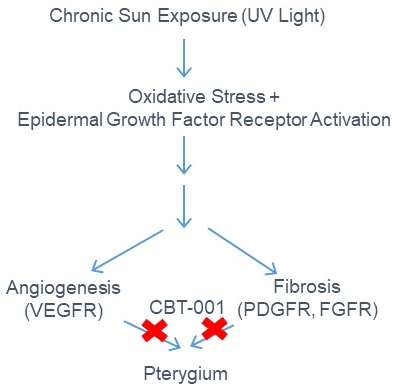
在2期臨床試驗中,與對照組相比,CBT-001顯著減少了翼狀胬肉血管和結膜充血,還顯著減少了角膜病變長度。此外,CBT-001在眼睛和全身中耐受性良好。沒有患者因不良反應而退出。沒有嚴重的藥物反應或不良反應。我們與FDA成功舉行了EOP2會議。3期研究計劃已提交特殊協定評估(SPA),FDA同意我們的3期研究計劃。
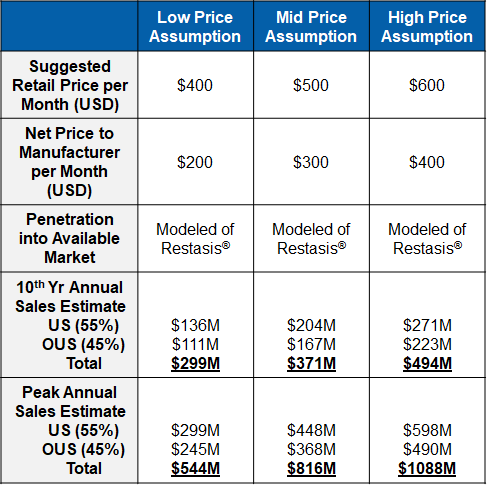
Market research supports a robust sales forecast for CBT-001 for the following reasons:
© 2025 Cloudbreak Pharma All Rights Reserved.