CBT-001
A potential first-in-class treatment for patients with pterygium
CBT-011 is currently in a Phase 3 clinical trial (NCT05456425) as a disease-modifying eyedrop therapy for pterygium.
突破性創新
Our Core Product CBT-001 is a potential first-in-class drug therapy using a multi-kinase inhibitor targeting platelet-derived growth factor receptors (“PDGFRs”), fibroblast growth factor receptors (“FGFRs”), and vascular endothelial growth factor receptors (“VEGFRs”). This unique eye drop is being developed as a treatment for pterygium, including reducing the size of the lesion as well as common, bothersome symptoms.
To our knowledge, there is currently no approved drug therapy for the treatment of pterygium globally, and the current existing treatment option for pterygium is surgical excision. If approved, CBT-001 is expected to be the first drug therapy globally for the treatment of pterygium and related bothersome symptoms, and to potentially reduce or postpone the need for surgical excision.
有藥物效性能與安全性
2 期臨床試驗7
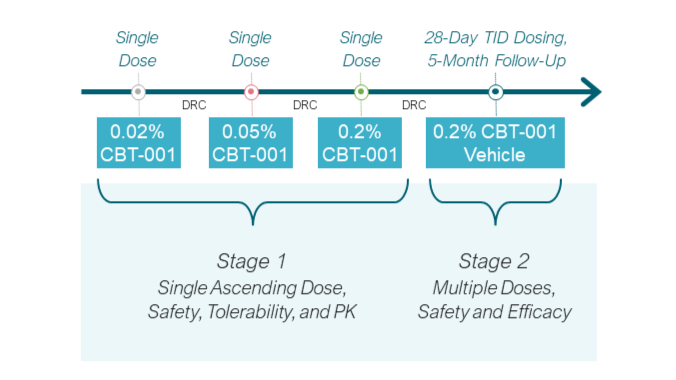
2期臨床試驗NCT03049852分為兩個階段。 第一階段包括對24名患者進行CBT-001劑量遞增,以確定最大耐受劑量。 結果證明瞭眼部安全性和耐受性,全身藥物暴露可忽略不計。 在第 2 階段,51 名患者接受了為期 4 周的 TID 週期 CBT-001 (n=25) 或載體 (n=23) 給葯治療,並隨訪至第 24 周。 到第 4 周,用藥組的平均血管分佈評分比對照組顯著下降, 並一直持續到第 16 周。 此外,在第 4 周觀察到病灶長度的平均變化比對照組明顯減少,並一直持續到第 8周。7
CBT-001 具有良好的耐受性,CBT-001 組中常見報告的大多數不良事件是眼部不良事件,嚴重程度較輕,並在治療后得到緩解。 沒有患者因不良事件而停止 CBT-001 治療。7
3期臨床試驗8
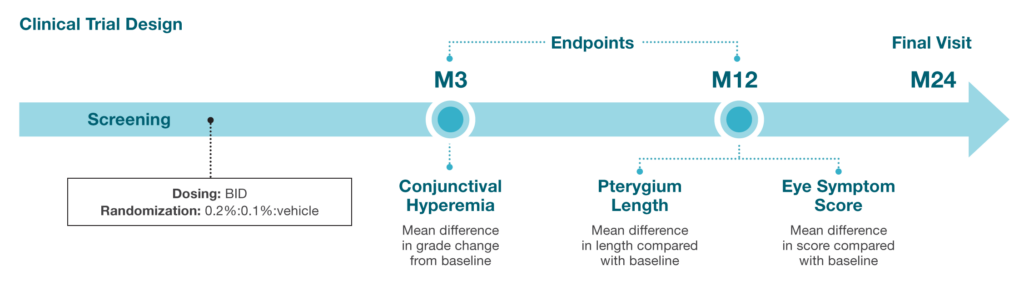
3期臨床試驗 (NCT05456425) is designed to evaluate the efficacy and safety of CBT-001 in patients with pterygium.8
方案標題:對翼狀胬肉患者進行多中心、雙盲、隨機、載體對照 12 個月平行比較 0.1% 和 0.2% CBT-001 與載體(每天給葯兩次)的安全性和有效性
研究目的:評估 0.1% 和 0.2% CBT-001 乳劑每天兩次給葯,持續 24 個月,與載體相比,在減少翼狀胬肉眼結膜充血和預防翼狀胬肉進展方面的安全性和有效性
目標入組:600 名患者
主要納入標準:
- 年齡≥12歲的男性或女性
- 角膜上方翼狀胬肉病變長度≥1.2毫米
- ≥3級結膜充血
主要排除標準:
- 過去 6 個月內進行過翼狀胬肉切除手術
- 預期在研究入組一年內進行翼狀胬肉手術
- 除翼狀胬肉以外的具有臨床意義的角膜異常
This Phase 3 clinical trial is fully enrolled with a data readout expected 3Q2026.
BID, twice daily; DRC, data review committee; FGFR, fibroblast growth factor receptor; M, month; PDGFR, platelet-derived growth factor receptor; PK, pharmacokinetics; TID, three times daily; VEGFR, vascular endothelial growth factor receptor.
1. Shahraki T, et al. Ther Adv Ophthalmol. 2021;13:25158414211020152. 2. Chu WK, et al. Eye (Lond). 2020;34(6):1047-1050. 3. Wanzeler ACV, et al. Clin Ophthalmol. 2018;12:833-837. 4. Palewski M, et al. Int J Environ Res Public Health. 2022;19:11357. 5. Hilberg F, et al. Cancer Res. 2008;68:4774–4782. 6. Yang R, et al. Invest Ophthalmol Vis Sci .2019;60(9):2087. 7. Whitcup SM, et al. Ophthalmol Sci. 2024. Publication in press. https://doi.org/10.1016/j.xops.2024.100502. 8. ClinicalTrials.gov. A clinical trial on safety and efficacy of CBT-001 in patients with pterygium. Updated March 15, 2024. Accessed March 15, 2024. https://clinicaltrials.gov/study/NCT05456425.