我們的產品在美國臨床試驗中
臨床試驗是旨在確定藥物對患者是否安全有效的研究。
Phase 3 評估 CBT-001 在翼狀胬肉患者中的療效和安全性的研究
狀況: 血管化的瞼裂斑
階段:第 3 階段
之前的 2 期研究已經完成。在該研究中,CBT-001眼科溶液分兩個階段進行了評估。第 1 階段是一項單次遞增劑量研究,以評估 0.02%、0.05% 和 0.2% CBT-001 的安全性、有效性和藥代動力學。)第 2 階段評估了 0.2% CBT-001 的療效和安全性,每天給葯 3 次 (TID),持續 4 周,隨訪 5 個月。主要終點是減少翼狀胬肉血管分佈,關鍵次要終點是抑制病變生長。兩個終點均顯示陽性結果。研究結果可以在 ClinicalTrials.gov 上找到。試驗完成後,我們與FDA成功舉行了EOP2會議。
3期研究已提交SPA,FDA接受了修改後的方案。
3 期研究標題:多中心、雙盲、隨機、載體對照 12 個月(12 個月,雙盲擴展)對 0.1% 和 0.2% CBT-001 的安全性和有效性的平行比較,每天給葯兩次,在翼狀胬肉患者中。
目的是評估 0.1% 和 0.2% CBT-001 乳液與載體相比,每天兩次給藥 24 個月在減少翼狀胬肉眼中的結膜充血和預防翼狀胬肉進展方面的安全性和有效性。
主要療效終點集中在減少由翼狀胬肉引起的結膜充血和抑制病變長度增加進展。
有關此 3 期研究的更多詳細資訊,請訪問 https://clinicaltrials.gov/study/NCT05456425
A second Phase 3 study is planned for early 2026. Please check ClinicalTrials.gov for more details.
Study Design
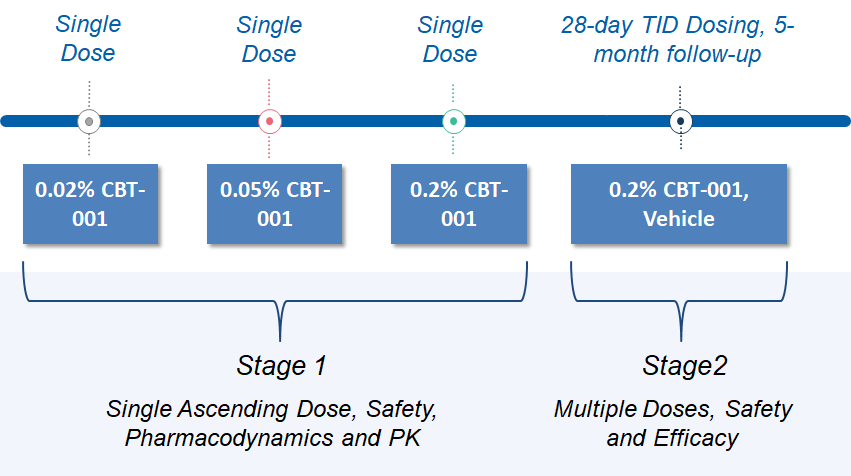
Please visit clinical trials.gov website to learn more about CBT-001 trial, and our Patient Information page to learn more about pterygium.
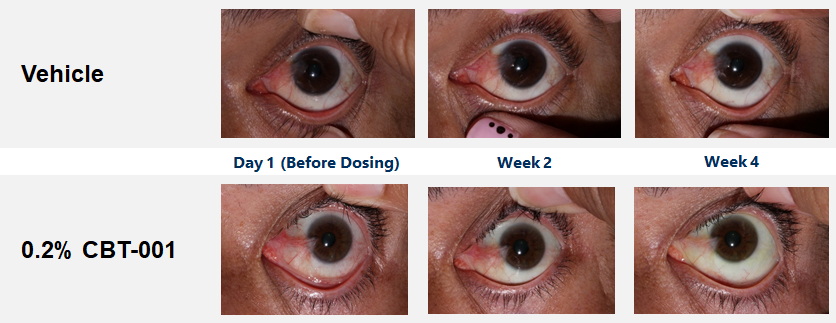
Primary Endpoint was Met with Highly Statistical Significance
CBT-001 demonstrates good ocular and systemic safety, quick onset, and highly effective during and post-dosing.
Baseline demographic characteristics were similar between patients receiving CBT-001 (n=25) and vehicle (n=23). After four (4) weeks of dosing, mean vascularity scores were significantly decreased in patients receiving CBT-001 (-0.8) compared to vehicle (0.0) (p<0.001). Vascularity remained significantly decreased at weeks 8 (p=0.008) and 16 (p<0.001), but not at week 24. The CBT-001 group showed significantly greater mean reductions in lesion length at week 2 (p=0.005), week 4 (p=0.007) and week 8 (p=0.0145).
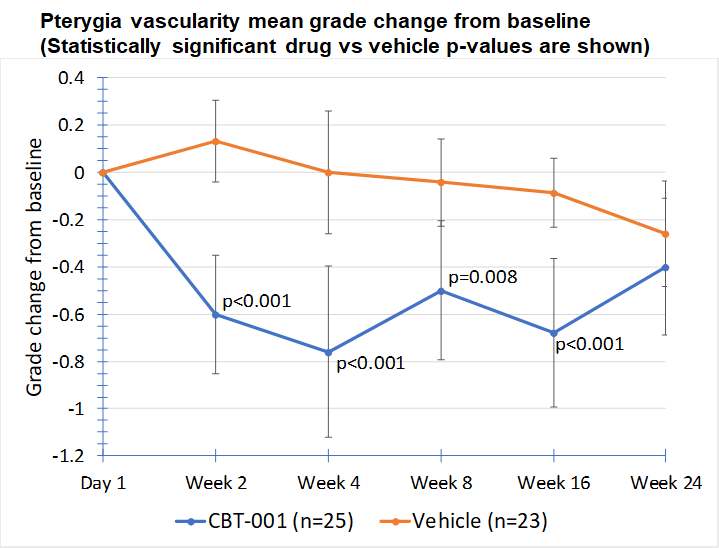
EOP2 Meeting with FDA
Proceed with Phase III Trials after a Successful EOP2 Meeting with FDA Regarding CBT-001 as a Treatment for Pterygium
We had a successful EOP2 meeting with the FDA. The FDA agreed with proceeding to Phase III trials, agreed on Phase III study design and efficacy endpoints, and agreed on CMC, non-clinical, and clinical plan.